
- DAZ.online
- DAZ / AZ
- DAZ 37/2020
- Überfordert und ...
Pandemie Spezial
Überfordert und unausgereift
Immunsystem verliert bei schweren COVID-19-Verläufen die Balance
Um genauer beurteilen zu können, welche komplexen immunologischen Mechanismen auf molekularer Ebene den Verlauf und die Pathologie einer COVID-19-Erkrankung prägen, führten Berliner, Leipziger und Heidelberger Wissenschaftler sogenannte Einzelzellanalysen bei 19 moderat bis schwer erkrankten und fünf nicht infizierten Probanden durch [1]. Insgesamt konnte aus den beprobten oberen und unteren Atemwegen die RNA von respektablen 160.528 Zellen sequenziert und analysiert werden. Die Studie brachte gleich mehrere erstaunliche Ergebnisse zutage.
Laute Hilferufe
Kritisch Erkrankte (n=11) zeigten im Vergleich zu moderat Betroffenen (n=8) ausgeprägtere Interaktionen zwischen Epithel- und Immunzellen. Zwar sind diese Interaktionen zur Aktivierung von Immunzellen – vermittelt über Zytokinausschüttung und Zell-Zell-Kontakte – erforderlich, um die Ausbreitung einer viralen Infektion unter Kontrolle zu bringen. Allerdings kann dies auch zu einem Überschießen des Immunsystems führen. Letzteres wird insbesondere dann beobachtet, wenn die herbeigerufenen, aktivierten Immunzellen im Anschluss an die virale Clearance nicht eliminiert werden, sondern bestehen bleiben und so nicht infiziertes Gewebe und Zellen schädigen können. In der vorliegenden Arbeit korrelierte die Schwere der kritischen Erkrankung, neben den vermehrten Interaktionen zwischen Epithel- und Immunzellen, also einem verstärkten „Hilferuf“ der körpereigenen Zellen, auch mit einer erhöhten Rate eben jener Immunzellen. Hauptsächlich handelte es sich um Makrophagen, die proinflammatorische Chemokine freisetzen, und zytotoxische T-Zellen, die für die Apoptose infizierter Zellen verantwortlich sind, aber auch bei überaktiviertem Immunsystem körpereigene Zellen angreifen können.
Erleichterter Eintritt
Zudem wurde ein besonders bemerkenswerter Nachweis erbracht. Bestimmte Epithelzellen in den oberen Atemwegen der COVID-19-Erkrankten waren im Vergleich zu Nichtinfizierten empfänglicher für die virale Infektion. Sie exprimierten den für den viralen Eintritt entscheidenden ACE-2-Rezeptor sowie mindestens eine der zur Aktivierung des Spike-Proteins erforderlichen Proteasen Furin und TMPRSS2 dreimal häufiger als vergleichbare Zellen nicht infizierter Kontrollpersonen. Tatsächlich waren es auch diese spezialisierten Epithelzellen, die bei den Erkrankten den höchsten Anteil SARS-CoV-2-infizierter Zellen stellten. Da eine ACE-2-Rezeptor-Expression unter anderem durch Interferone getriggert wird, welche wichtige Botenstoffe bei der Infektion sind, lässt sich gut nachvollziehen, weshalb es zu dieser denkbar unglücklichen Situation kommt.
Dysreguliertes Immunsystem?
Die Deutsche COVID-19 OMICS Initiative (DeCOI) ging in einer weiteren Untersuchung der Frage nach, weshalb genau die lauten Hilferufe des Immunsystems schwer erkrankter COVID-19-Patienten scheinbar verhallen und sich klinisch immer wieder das Bild einer ineffektiven Immunantwort darbietet. Sie analysierten 161 Blutproben von 53 mild oder schwer erkrankten Berliner und Bonner COVID-19-Patienten sowie 81 Blutproben von 56 Kontrollen hinsichtlich Unterschieden in der Zusammensetzung und dem Reifestatus von Immunzellen [2]. Dabei verfolgten sie die Hypothese, dass Unterschiede im klinischen Verlauf einer COVID-19-Erkrankung in abweichenden Immunantworten, insbesondere des angeborenen Immunsystems, begründet sind.
Bei schweren COVID-19-Verläufen imponierten erhöhte Leukozyten- und Neutrophilen-Werte im Blut, kennzeichnend für eine hohe Entzündungsaktivität, während bei milden Verläufen nur eine Zunahme der neutrophilen Granulozyten zu verzeichnen war. COVID-19-Patienten beider Gruppen wiesen zudem eine Lymphopenie auf.
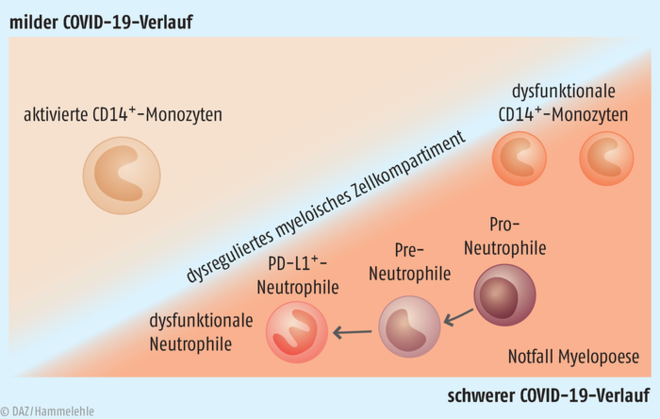
Abb: Unterschiede in der Krankheitsschwere von COVID-19 sind unter anderem in Dysregulationen des angeborenen Immunsystems begründet und äußern sich in abweichender Zusammensetzung und dem Reifestatus der myeloiden Zellen. Während bei milden Verläufen aktivierte CD14+-Monozyten vorlagen, die eine kompetente Immunantwort erlauben, waren diese bei schweren Verläufen nur unzureichend aktiviert. Charakteristisch für die Notfall-Myelopoese waren zudem unreife Neutrophilen-Vorstufen. Das Auftreten von Neutrophilen, die das Oberflächenprotein PD-L1 (Programmed Death Ligand 1) exprimieren, ist ein weiteres Indiz dafür, wie eine SARS-CoV-2-Infektion das Immunsystem ausbremst (adaptiert nach [2]).
Aktivierung und Differenzierung fehlen
In Abhängigkeit der Krankheitsschwere zeigte sich jedoch eine Besonderheit: Das Monozytenkompartiment, aus dem sich zum Beispiel die für die virale Phagozytose wichtigen Makrophagen rekrutieren, wies im Vergleich zu Gesunden deutliche Veränderungen auf. Bei schwer erkrankten COVID-19-Patienten konnte – ähnlich wie bei septischen Krankheitsverläufen – eine unzureichende Monozyten-Aktivierung festgestellt werden, zudem traten unreife und in ihrer Funktion gestörte Vorstufen von Neutrophilen auf, welche immunsuppressiv wirken können. Die schnelle Mobilisierung unreifer myeloischer Zellen wird auch als Notfall-Myelopoese bezeichnet (Abb.). Bei milden Verläufen waren die Monozyten und Neutrophilen hingegen aktiviert und funktionsfähig, sodass nachfolgende Prozesse in der Immunabwehr ungestört ablaufen konnten. Vermutlich stellt bei schweren Verläufen die Bereitstellung nicht ausreichend aktivierter und differenzierter Immunzellen ein großes Hindernis in der Infektabwehr dar und trägt entscheidend zur dysfunktionalen Antwort des angeborenen Immunsystems und daran anschließender Kaskaden bei. Da den meisten Patienten mehrfach Blut abgenommen wurde, gelang bei schwer Erkrankten sogar der Nachweis, dass mit zunehmendem Krankheitsverlauf immer mehr unreife Neutrophile freigesetzt werden. Die Studienergebnisse erhärten den Verdacht, dass sich der Körper massiv gegen die starke Entzündung im Lungengewebe und im systemischen Kreislauf zu wehren versucht, sich aber mit den ergriffenen Maßnahmen scheinbar im Kreis dreht. |
Literatur
[1] Chua RL et al. COVID-19 severity correlates with airway epithelium-immune cell interactions identified by single-cell analysis. Nat Biotechnol. 2020;38(8):970-979. doi: 10.1038/s41587-020-0602-4.
[2] Schulte-Schrepping et al. Severe COVID-19 Is Marked by a Dysregulated Myeloid Cell Compartment. Cell 2020;182:1–22. https://doi.org/10.1016/j.cell.2020.08.001
Immunantwort außer Kontrolle – drei Fragen an Prof. Dr. Leif Erik Sander
Der Internist und Pneumologe Prof. Dr. Leif Erik Sander von der Charité – Universitätsmedizin Berlin ist Mitglied des Steering Committes des Charité Corona Research Boards und erforscht als Leiter der Forschungsgruppe „Infektionsimmunologie und Impfstoffforschung“ unter anderem die Immunantwort auf SARS-CoV-2. Er steht auch im Rahmen des wissenschaftlichen eKongresses der Interpharm online (www.interpharm.de) am 25. September Rede und Antwort zu COVID-19. Hier ein kleiner Vorgeschmack.
DAZ: Viele aktuelle Forschungsergebnisse sprechen für ein ausgeprägt dysreguliertes Immunsystem bei schweren COVID-19-Verläufen. Welcher Schritt der Immunantwort gerät dabei besonders außer Kontrolle?
Sander: Das betrifft viele Aspekte der Immunantwort, aber v. a. fallen bei diesen Patient*innen Zellen des angeborenen Immunsystems mit einem unreifen und dysfunktionalen Phänotyp auf.
DAZ: Kann das Auftreten potenziell dysfunktionaler, unreifer Neutrophile bei schwer erkrankten COVID-19-Patienten unter diagnostischen Routinebedingungen erfasst werden?
Sander: Ja, das kann mit modernen Blutbildgeräten im Routinelabor erfasst werden. Das konnten wir an unserer Berliner Patienten-Kohorte zeigen. Nun müssen wir prüfen, ob der Nachweis von unreifen Neutrophilen auch einen prädiktiven Wert für den Krankheitsverlauf hat.
DAZ: Sind pharmakologische Angriffspunkte denkbar, um die wichtige immunologische Balance wiederherzustellen?
Sander: Wir glauben, dass es in der Tat pharmakologische Angriffspunkte gibt. Aktuell läuft an der Charité dazu eine Studie mit einem Chemokin-Rezeptorantagonisten. Dadurch soll der übermäßige Einstrom von dysregulierten Monozyten in das Lungengewebe verhindert und so die Lungenschädigung minimiert werden.























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.