
- DAZ.online
- News
- Recht
- Wirrwarr um Notfall- und...
COVID-19-Impfstoff
Wirrwarr um Notfall- und „ordentliche“ Zulassungen
Remagen - 21.12.2020, 17:50 Uhr
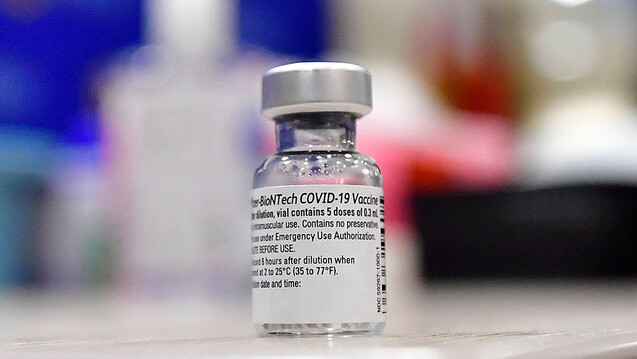
Seit 18. Dezember können die Vereinigten Staaten mit zwei Corona-Impfstoffen gegen COVID-19 impfen: Die FDA erteilte der Moderna-Vakzine mRNA-1273 am Freitag die Notfallzulassung – nur eine Woche nach der Notfallzulassung für BNT162b2 von Biontech/Pfizer. (Foto: imago images / ZUMA Press)
Notfallgenehmigung in Deutschland schon früh angedacht
In Deutschland können die zuständigen Behörden in Krisenzeiten bei einer Pandemie im Einzelfall gestatten, dass Arzneimittel, die hierzulande nicht zugelassen sind, befristet in den Verkehr gebracht werden (§ 79 Abs. 5 AMG). Dies gilt im Falle eines Versorgungsmangels mit den Arzneimitteln, die für die Vorbeugung oder Behandlung einer bedrohlichen übertragbaren Krankheit benötigt werden. Das BMG hatte einen solchen Versorgungsmangel mit Blick auf das neuartige Coronavirus (COVID-19) vorsorglich schon am 27. Februar 2020 bekannt gemacht, will den Weg der Sondergenehmigung aktuell aber nicht beschreiten, wie Jens Spahn immer wieder betont. Stattdessen hält man an dem einheitlichen europäischen Weg fest, von dem sich die Länder eine höhere Verlässlichkeit des Verfahrens versprechen.
Eingehendere Prüfung und einhellige Bewertung
Zwischen einer bedingten EU-Marktzulassung und nationalen Notfallzulassungen gibt es wesentliche Unterschiede. So muss bei einer bedingten Marktzulassung der ganze Katalog an Daten und Unterlagen, den das strenge EU-Zulassungsrecht vorsieht, vorgelegt und im Detail geprüft werden. Bei einer nationalen Notfallzulassung entscheidet ein Mitgliedstaat dagegen selbst darüber, welche Daten für eine solche Zulassung erforderlich sind und welche Anforderungen er an die Verwendung und Überwachung des Impfstoffs stellt. Hier können unter Umständen Abstriche gemacht werden, beispielsweise in Bezug auf den Umfang der klinischen Daten und Wirksamkeitsanalysen. Die EU-Kommission betont in ihren Erläuterungen, dass die behördliche Beurteilung der Daten deswegen mehr Zeit benötigen kann als ein Notfallzulassungsverfahren. Außerdem sind an der Überprüfung zentraler Zulassungsanträge regelmäßig viele Experten aus allen Mitgliedstaaten beteiligt. Das heißt, es muss ein weitreichender Konsens hergestellt werden.
Die Krux der Haftung
Es gibt aber noch einen weiteren wesentlichen Unterschied, nämlich die Haftungsfrage. Bei einer bedingten EU-Marktzulassung haftet wie bei einer „normalen“ Zulassung deren Inhaber, also das herstellende Pharmaunternehmen. Im Falle einer Notfallzulassung für den vorübergehenden Vertrieb als nicht zugelassenes Produkt müssen die Mitgliedstaaten den Hersteller wie auch den Verantwortlichen für das Inverkehrbringen nach EU-Recht von der administrativen und zivilrechtlichen Haftung ausnehmen, wenn sie eine solche Notfallverwendung empfehlen oder vorschreiben. Dies dürfte für die Länder, die sich bei der Zulassung von COVID-19-Impfstoffen klipp und klar für die europäische Lösung ausgesprochen haben, ebenfalls eine maßgebliche Rolle spielen.
Zulassung schnellstmöglich
Die EMA hatte angekündigt, die Prüfung des COVID-19-Impfstoffs von Biontech/Pfizer am 21. Dezember in einem Sonder-Meeting abschließen zu wollen. Nach der nun positiven Empfehlung des Ausschusses für Humanarzneimittel (CHMP) der EMA will die Kommission die Marktzulassung des Impfstoffes schnellstmöglich beschließen. Dafür muss sie auch noch einmal die Mitgliedstaaten konsultieren. Wenn diese die Zulassung mit qualifizierter Mehrheit befürworten, kann die EU-weite Vermarktung des Impfstoffs genehmigt werden.
Die Anwender und Empfänger der Impfstoffe können sich am Ende darauf verlassen, dass bei dem Verfahren alle „Netze und doppelten Böden“ genutzt wurden, die aktuell in dieser unsicheren Lage zur Verfügung stehen.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.