
- DAZ.online
- News
- Pharmazie
- Große Probleme mit ...
Notfallbevorratung
Große Probleme mit Diphtherie-Antitoxin in Deutschland
Stuttgart - 14.08.2017, 07:00 Uhr
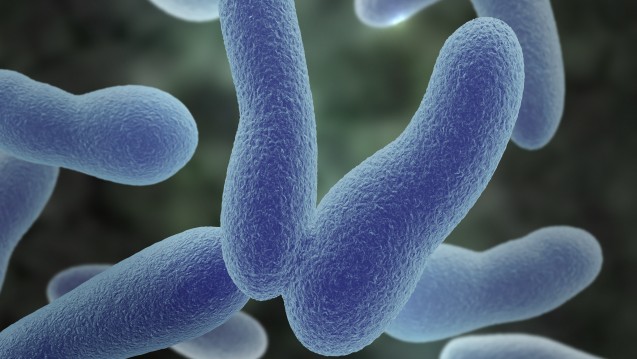
Das Bakterium Corynebacterium diphtheriae – nach den Entdeckern auch Klebs-Loeffler-Bazillus genannt – löst die Diphtherie aus. (Foto: Sagittaria / Fotolia)
Schon seit Jahren sieht es schlecht aus mit der Bevorratung des Diphtherie-Antitoxins. Nach Recherchen von DAZ.online hat sich die Lage zugespitzt: Da kein zugelassenes Arzneimittel verfügbar ist, müssen bedenkliche Präparate aus Russland oder Indien importiert werden. Die Haftung liegt im Regelfall bei Apothekern und Ärzten.
Die Diphtherie ist durch flächendeckende Impfungen in Deutschland weitgehend im Griff, es gibt jedes Jahr nur wenige Infektionen. Doch die Zahlen steigen: Während in den zehn Jahren 2002 bis 2011 insgesamt nur 21 Fälle in der Datenbank des Robert-Koch-Instituts verzeichnet sind, waren es in den vergangen fünf Jahren 2012 bis 2016 insgesamt 45 Diphtheriefälle in Deutschland. Für Patienten, bei denen es zu schweren Symptomen kommt, ist die gesetzlich vorgeschrieben Notfallbevorratung mit dem Dipththerie-Antitoxin teils überlebenswichtig, das die Sterblichkeit erheblich reduzieren kann.
Doch weltweit gibt es seit vielen Jahren Probleme bei der Beschaffung des Arzneimittels. Nach einem WHO-Bericht vom Februar ist die Zahl der mit Diphtherie infizierten Patienten von 100.000 pro Jahr auf rund 5000 pro Jahr zurückgegangen – doch die WHO äußert auch ihre „Besorgnis über die berichteten Engpässe“ beim Diphtherie-Antitoxin. So ist beispielsweise ein Fall aus Spanien bekannt, wo ein an Diphtherie erkrankter 6-jähriger Junge drei Tage nur mit Anitbiotika behandelt werden konnte, da das Antitoxin nicht zur Verfügung stand.
Der Wirkstoff wird von der WHO auf der Liste der essenziellen Arzneimittel aufgeführt. Bei einer Befragung im vergangenen Jahr durch die WHO haben jedoch nur drei Hersteller angegeben, das Antitoxin verfügbar zu haben: Ein Staatsbetrieb sowie ein privates Unternehmen in Indien, sowie ein Staatsbetrieb in Russland, der zum Gesundheitsministerium gehört. In Indonesien stellt außerdem ein Impf-Hersteller und in Brasilien das angesehene Forschungsinstitut „Instituto Butantan“ das Antitoxin her, doch beide nur für den nationalen Markt. Inwiefern vier weitere Hersteller in Bulgarien, Japan, Kroatien und Schweden das früher von den Behringwerken hergestellte Arzneimittel liefern können, blieb unklar.
Ein erhebliches Problem gibt es bei allen Produkten, wie DAZ.online auf Nachfrage beim Bundesgesundheitsministerium (BMG) und bei mehreren Landesministerien erfährt. „In der EU sind derzeit keine zugelassenen Arzneimittel mit Diphtherie-Antitoxin erhältlich“, erklärt ein Sprecher von Bundesgesundheitsminister Hermann Gröhe (CDU). Die Neubeschaffung gestalte sich „schwierig“.
Haftung liegt beim Arzt oder Apotheker
Nach Angaben mehrerer Apothekerkammern ist das Problem erheblich, denn sie müssen die Arzneimittel einlagern. So bestehen pharmazeutische Bedenken gegen die Produkte – sie sind schlichtweg nicht verkehrsfähig. Haftungsrisiken liegen zunächst bei den Kammern. Ausnahmeregeln im Arzneimittelgesetz gestatten unter gewissen Bedingungen zwar die Einfuhr, bestätigt das Bayerische Gesundheitsministerium auf Nachfrage – doch: „Die Produkthaftung für die Importe liegt nicht beim pharmazeutischen Unternehmer, sondern beim Arzt und Apotheker.“
Zwar gäbe es „derzeit noch“ Vorräte des Diphtherie-Antitoxins, die im Bedarfsfall eingesetzt werden können – was in den vergangenen Jahren in ungefähr zwei Fällen pro Jahr passierte. Doch auch die Gesundheitsministerkonferenz (GMK) betrachte den derzeitigen Versorgungsmangel mit Diphtherie-Antitoxin auf europäischer Ebene „mit großer Sorge“, betont das Ministerium. Weiterhin müsse mit Einzelfällen gerechnet werden, bei denen die frühzeitige Einleitung der Therapie mit Diphtherie-Antitoxin lebensrettend sein könne. „Die GMK bittet die Bundesregierung, kurzfristig auch auf europäischer Ebene Lösungswege zu entwickeln, um dem aktuellen Versorgungsmangel konkret begegnen zu können“, heißt es.
Auch im Nachbarland Baden-Württemberg betreibt die Landesapothekerkammer Notfalldepots. Dass in Russland und Indien hergestellte Antitoxin entspräche nicht den in Europa vorgeschriebenen pharmazeutischen Spezifikationen, betont das dortige Gesundheitsministerium auf Nachfrage. Auch hier verweist das Ministerium auf die Verantwortung der Heilberufler. „Sofern ausschließlich ein qualitätsgemindertes oder nicht zugelassenes Produkt zur Verfügung steht muss der behandelnde Arzt über den Sachverhalt informiert werden und nach sorgfältiger Abwägung der Umstände des Einzelfalls eine sachgerechte Entscheidung im Sinne des Patienten treffen“, erklärt ein Pressesprecher.
Zuletzt seien im Jahr 2013 fünf Ampullen Diphtherie-Antitoxin aus den Notfalldepots entnommen worden. „Baden-Württemberg bemüht sich gemeinsam mit dem Bundesministerium für Gesundheit, den übrigen Bundesländern und der Arbeitsgemeinschaft Deutscher Apothekerverbände um eine nachhaltige Lösung mit Blick auf die Sicherstellung der Notfallbevorratung“, erklärt das Ministerium – und verweist auf die Möglichkeit der Impfung gegen Diphtherie.
Firmen können nicht zur Herstellung gezwungen werden
In Sachsen wird das Antitoxin in drei Notfalldepots in Krankenhausapotheken vorgehalten. Bei Notfallarzneimitteln, die über die Sonderregelung trotz fehlender Zulassung importiert werden dürfen, entfalle die Gefährdungshaftung durch den pharmazeutischen Unternehmer, erklärt das sächsische Gesundheitsministerium auf Nachfrage. Stattdessen hafte der einführende Apotheker, wie sich auf dem Produkthaftungsgesetz und dem Bürgerlichen Gesetzbuch ergebe.
Die Versorgungssituation mit Diphtherie-Antitoxin bezeichnet das Ministerium als „unzureichend“. „Eine Einflussmöglichkeit der für die Arzneimittelüberwachung zuständigen Behörden auf die Produktionspalette pharmazeutischer Unternehmer (zum Beispiel Maßnahmen gegen Produktionseinstellungen) bestehen jedoch nach dem geltenden Arzneimittelrecht nicht“, erklärt ein Sprecher. Somit sei die Apothekerkammer darauf angewiesen, die nicht zugelassenen Arzneimittel aus dem Ausland zu importieren.
Auch in Hessen wird darauf verwiesen, dass der individuelle Einsatz des nicht zugelassenen Arzneimittels unter der unmittelbaren Verantwortung des Arztes erfolge – der seine ärztliche Aufklärungspflicht verletzt, wenn er den Patienten nicht darüber informiert, dass das Arzneimittel nicht zugelassen. Auch haften Ärzte dem Patienten auf Schadenersatz. „Deshalb ist die Abgabe des Diphtherie-Antitoxins in Hessen zwingend an die Information des Arztes und die Aufklärung des Patienten geknüpft“, erklärt ein Sprecher des hessischen Gesundheitsministeriums. „Die Landesapothekerkammer stellt für diesen Fall entsprechendes Informationsmaterial zur Verfügung.“
Auf Nachfrage, wie das BMG auf die Probleme mit der Notfallbevorratung reagieren will, verweist eine Sprecherin lediglich auf die ABDA. Diese prüfe „fortlaufend mögliche Bezugsquellen für Diphtherie-Antitoxin in akzeptabler pharmazeutischer Qualität“, erklärt das Ministerium. „Hierbei wird sie vom BMG und vom Paul-Ehrlich-Institut im Rahmen der jeweiligen Möglichkeiten unterstützt.“
Und wie bewertet die ABDA die Probleme, auch hinsichtlich der Haftungsrisiken – und welche Lösungsansätze kann sie sich vorstellen? Die Antwort fällt kurz aus: Die Apothekerkammern der Länder stünden „mit den zuständigen Stellen in ständigem Kontakt“, erklärt ein Sprecher.


























1 Kommentar
Haftung bei uns - und nun?
von Sven Larisch am 14.08.2017 um 9:26 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.