
- DAZ.online
- News
- Pharmazie
- Vielfältige Darmflora...
Checkpoint-inhibitoren
Vielfältige Darmflora – bessere anti-Tumorwirkung
Houston/Villejuif/Heidelberg - 06.11.2017, 09:00 Uhr
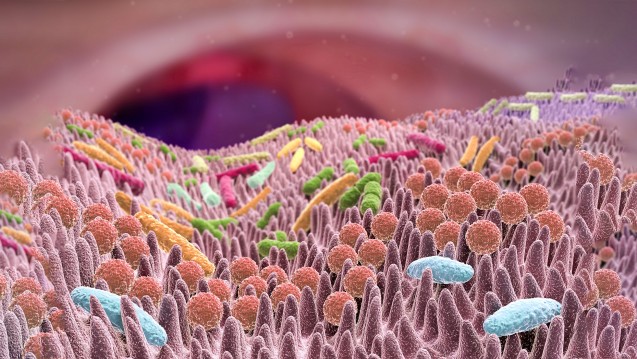
Die Darmflora beeinflusst die Wirkung von Arzneistoffen, anscheinend auch die der Checkpoint-Inhibitoren. (Foto: Alex / stock.adobe.com)
Immuntherapien mit den sogenannten Checkpoint-Inhibitoren werden unter anderem derzeit bei der Behandlung von Melanomen oder beim nicht-kleinzelligen Lungenkarzinomen eingesetzt. Anscheinend beeinflusst die Zusammensetzung der Darmflora den Therapieerfolg. Das berichten zwei Forschergruppen aus den USA und Frankreich in „Science“ unabhängig voneinander. Demnach scheint ein vielfältiges Mikrobiom von Vorteil zu sein, Antibiotikabehandlungen hingegen wirkten sich in den Untersuchungen nachteilig aus.
Checkpoint-Inhibitoren sind innerhalb der Europäischen Union bislang für fortgeschrittene Krebserkrankungen zugelassen, zum Beispiel Ipilimumab (Yervoy®) zur Behandlung von Patienten mit metastasiertem schwarzem Hautkrebs, Nivolumab (Opdivo®) unter anderem bei metastasiertem und/oder inoperablen Melanom, bei NSCLC, Nierenzell- und Urothelkarzinomen und Pembrolizumab (Keytruda®) unter anderem für Patienten mit inoperablen Melanomen oder Fernmetastasen, NSCLC und Urothelkarzinom.
Seit September dieses Jahres bereichern zwei weitere Checkpoint-Inhibitoren die onkologischen Therapieoptionen: Avelumab (Bavencio®) hemmt PD-L1, also erstmalig den Liganden. Avelumab hat die Indikation zur Therapie der orphan disease Merkelzelkarzinom. Atezolizumab (Tecentriq®) von Roche hat die EMA-Zulassung für Urothelkarzinom und für NSCLC. Atezolizumab hemmt ebenfalls PD-L1.
Behandlung schlägt nicht immer an
Die neuen immuntherapeutischen Krebswirkstoffe bieten zwar Patienten, für die es bisher nur sehr eingeschränkte therapeutische Optionen gab, eine Perspektive, sie haben aber auch Schwächen. Eine davon ist, dass nicht jeder Betroffene darauf anspricht. Warum dies so ist, wird weltweit von zahlreichen Forschergruppen untersucht.
So auch vom US-Team um Jennifer Wargo vom Anderson Cancer Center der University of Texas in Houston. Diese Forscher analysierten bei 112 Melanom-Patienten, die eine Checkpoint-Inhibitor-Therapie bekamen, die Mikrobiome im Mundraum sowie im Darm. Die Mikroorganismen im Mund hatten keinen Einfluss auf den Behandlungserfolg. Dagegen fand das Team im Darm jener Patienten, bei denen die Behandlung anschlug, eine wesentlich reichhaltigere Flora und insbesondere Bakterien aus der Gruppe der Ruminococcaceae.
Zu einem ähnlichen Ergebnis kommt eine Arbeitsgruppe um Laurence Zitvogel vom französischen Gustave Roussy Cancer Center (GRCC) in Villejuif. Sie untersuchten knapp 250 Patienten mit Blasenkarzinom, nicht-kleinzelligem Lungenkarzinom (NSCLC) und Nierenzellkarzinom (RCC). Auch hier beeinflusste das Mikrobiom den Therapieerfolg. Dieser Studie zufolge ging insbesondere der Keim Akkermansia muciniphila, der in der Darmschleimhaut lebt, mit einem guten Ansprechen auf die Immuntherapie einher. Patienten, die Antibiotika bekamen, hatten dagegen häufiger Rückfälle und starben im Mittel früher.
Mehr zum Thema
Prüfen, ob man Darmflora gezielt verändern kann
Beide Forschergruppen untersuchten den Effekt der Darmflora auf die Immuntherapie auch an Mäusen. So verpflanzte das US-Team Darmbakterien von Patienten in bis dahin keimfreie Tiere. Erhielten die Mäuse Mikroorganismen von Patienten, die auf die Therapie angeschlagen hatten, so wuchsen Tumore bei ihnen langsamer. Die französische Gruppe zeigte dies ebenfalls. Verabreichten sie Mäusen, die nicht auf die Krebstherapie reagierten, den Keim Akkermansia muciniphila, so besserte sich die Erfolgsrate. „Wir folgern aus dieser Studie, dass das Darm-Mikrobiom das Ergebnis einer Checkpoint-Inhibitor-Therapie bei Mäusen und Patienten merklich verbessert“, betont die Gruppe.
Die US-Forscher wollen nun in einer weiteren Studie prüfen, ob und wie sich die Darmflora so verändern lässt, dass Immuntherapien optimal anschlagen. „Man kann das Mikrobiom verändern, das ist nicht schwierig“, wird Wargo in einer Mitteilung ihrer Universität zitiert. „Deshalb glauben wir, dass diese Resultate enorme Möglichkeiten eröffnen.“ Dies müsse unverzüglich geklärt, heißt es in „Science“.
Mehr zum Thema
Wird die Mikrofilm-Analyse Standard?
Jochen Sven Utikal, Leiter der Dermato-Onkologie am Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg, spricht von plausiblen Ergebnissen. Es sei bekannt, dass die Darmflora das Immunsystem aktiver und effektiver machen könne, dies könne auch gegen Tumore helfen. Derzeit sei die Analyse des Patienten-Mikrobioms außerhalb von Forschungsprojekten nicht üblich. Das könne aber angesichts der neuen Erkenntnisse bald Standard werden - sofern größere Studien die Resultate bestätigen. So könne man etwa prüfen, ob Kapseln mit bestimmten Darmbakterien die Erfolgsrate der Checkpoint-Inhibitor-Therapie steigern. „Dann könnte das sich sehr schnell etablieren“, sagt der Experte.
Körpereigener „Bremsmechanismus“
Auch andere Arbeitsgruppen konnten jüngst Ergebnisse in der Frage publizieren, welche Faktoren den Therapieerfolg beeinflussen. Ein internationales Forscherteam aus Deutschland, Australien und Belgien unter der Leitung von Michael Hölzel vom Institut für Klinische Chemie und Klinische Pharmakologie am Universitätsklinikum Bonn und Thomas Tüting von der Universitätshautklinik in Magdeburg hatte nun einen körpereigenen „Bremsmechanismus“ aufgedeckt, der die Wirksamkeit der Krebsimmuntherapie begrenzt. Diese Ergebnisse ihrer Studie sind im Fachjournal „Immunity“ erschienen.
Bei dem Bremsmechanismus kommt eine weitere Art von Immunzellen ins Spiel, die neutrophilen Granulozyten, die mit Abstand am häufigsten im Blut vorzufinden sind.





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.