
- DAZ.online
- News
- Apotheke
- Fragen und Antworten zu ...
Was Apotheker zum Start wissen müssen (teil 2)
Fragen und Antworten zu Securpharm
Stuttgart - 07.02.2019, 17:50 Uhr

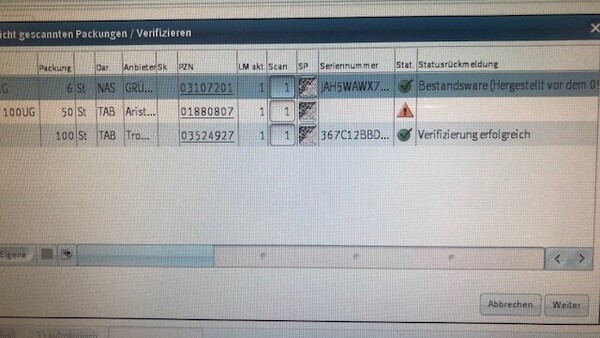
Mit der Musterpackung scheint alles ganz einfach, im Echtbetrieb gibt es dann doch viele Fragen (c / Foto: Securpharm)
Nimmt der Großhandel für die FAM-Prüfung geöffnete Packungen zurück?
Muss ich ein Arzneimittel nach negativer Verifizierung zwingend in der Apotheke aufbewahren oder kann ich es auch an den Lieferanten zurückgeben?
Diese Frage ist nicht abschließend geklärt. Laut Bundesgesundheitsministerium (BMG) soll das entsprechende Arzneimittel zunächst nicht an den Großhändler zurückgesendet werden. Das BMG begründet dies damit, dass es sich um ein Arzneimittel handelt, bei dem zumindest ein Anfangsverdacht besteht, dass es gefälscht sein könnte. Das sollte mindestens solange nicht in das Vertriebsnetz gelangen dürfen, bis die Entscheidung über das weitere Vorgehen getroffen wurde.
Außerdem geht das Ministerium davon aus, dass Securpharm das Ergebnis an die verifizierende Stelle zurückmeldet, sodass bei einer Rücksendung der Ware von der Apotheke an den Großhandel Informations- und Warenströme auseinanderlaufen würden.
Die ABDA meint dagegen, dass ein solches Arzneimittel durchaus auch an den Lieferanten zurückgegeben werden kann, es also zwei Handlungsoptionen gibt. So schreibt sie es auch in ihren FAQ und bestätigt es aktuell in einer Information zum „Umgang mit der Pflicht zur Separierung ab dem 9. Februar 2019“. Die technischen Möglichkeiten, auch bei einer Rücksendung die entsprechenden Daten abzurufen, um den Meldepflichten nachzukommen, soll die NGDA zur Verfügung stellen, heißt es. Die Entscheidung, wie er im Einzelfall vorgeht, sollte am Ende der Apothekenleiter in eigener Verantwortung treffen, meint die ABDA.
Derzeit lässt sich sagen: Mit der BMG-Empfehlung ist man jedenfalls auf der sicheren Seite.
Muss ich die getroffenen Maßnahmen nach einem Alarm dokumentieren?
Der neue § 21 ApBetrO schreibt vor, dass die getroffenen Maßnahmen in der Apotheke zu dokumentieren sind.
Was ist zu tun, wenn es neben der negativen Verifikation andere Indizien gibt, die auf einen Fälschungsverdachtsfall hindeuten?
Dann muss dies unmittelbar der Aufsichtsbehörde und der AMK gemeldet werden. Dann ist die 7-Tage-Regel hinfällig.
Mehr zum Thema

Wichtiges vor dem Start
Fertigarzneimittelprüfung und Securpharm – so geht’s
Ist der Erstöffnungsschutz einheitlich?
Nein, es kann verschiedene Varianten geben, zum Beispiel Klebesiegel, verklebte Packung mit perforierter Lasche oder Drehverschlüsse mit Sicherungsring.
Dürfen Apotheker die Packung zu Prüfzwecken öffnen?
Apotheker dürfen, wie bisher, die mit dem Erstöffnungsschutz versehene Packung zu Prüfzwecken im Rahmen der FAM-Prüfung gemäß ApoBetrO öffnen, wenn Sie die Packung nach positiver Prüfung entsprechend kennzeichnen. Diese Kennzeichnung ist bei Bedarf dem Patienten vor der Abgabe zu erklären. Ob es eine Änderung der Apothekenbetriebsordnung geben wird, ist derzeit nicht klar.
Chargenüberprüfungen werden wegen des finanziellen Risikos für die Apotheken nicht mehr empfohlen. Die entsprechenden Arzneimittel sollen durch die pharmazeutische Industrie stattdessen zurückgerufen werden, heißt es in den FAQ der ABDA.
Was passiert, wenn der Erstöffnungsschutz nicht intakt ist?
Wurde er in der Apotheke geöffnet, zum Beispiel für die Fertigarzneimittelprüfung, kann die Packung abgegeben werden. Die Packung muss dann entsprechend gekennzeichnet und der Bruch dokumentiert werden. Bei einem Bruch des Originalitätsverschlusses außerhalb des Kontrollbereichs der Apotheke, verliert die Packung ihre Abgabefähigkeit und muss als Fälschungsverdacht an die AMK und die zuständige Aufsichtsbehörde gemeldet werden.
Es gibt keinen Erstöffnungsschutz. Was tun?
Wenn es sich um Bestandsware oder OTC (außer Omeprazol) handelt, kann die Packung abgegeben werden. Ist das nicht Fall, muss sie als Fälschungsverdacht an die AMK und die zuständige Aufsichtsbehörde gemeldet werden.
Kann man für die FAM-Prüfung geöffnete Packungen an den Großhandel zurückgeben?
Die Großhändler erklären auf Nachfrage, dass sie diese Packungen nicht zurücknehmen, weil die Öffnung außerhalb ihres Kontrollbereichs stattgefunden hat. Es empfiehlt sich also in der Praxis, vor allem Packungen zu prüfen, die sicher verkauft werden, oder Arzneimittel ohne Erstöffnungsschutz.





























1 Kommentar
Bestandsware
von Stefan Schwenzer am 07.02.2019 um 21:46 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.