
- DAZ.online
- News
- Pharmazie
- Was die Chinesen zu ...
Corona-Impfstoffe
Was die Chinesen zu bieten haben
Remagen - 12.02.2021, 17:55 Uhr
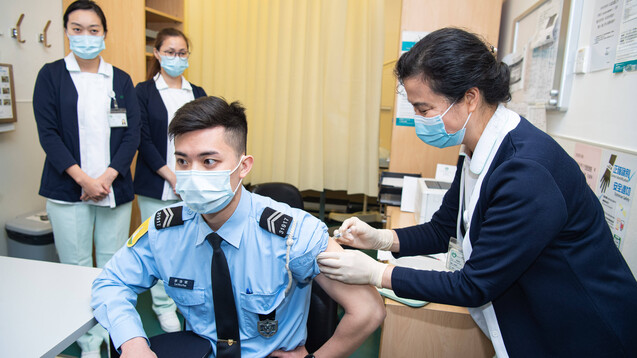
Die Notfallgenehmigungen in China sollten die Verwendung von Impfstoffkandidaten für einen begrenzten Zeitraum bei Personen mit einem hohen COVID-19-Erkrankungsrisiko ermöglichen. Dazu gehörten medizinisches Personal, Mitarbeiter:innen der Pandemiekontrolle und Zollarbeiter:innen. (Foto: IMAGO / Xinhua)
Mittlerweile breiten sich neben dem Corona-Virus selbst auch die Notfallzulassungen für COVID-19-Vakzine sukzessive über die Weltkarte aus. China versucht derzeit, drei Impfstoffe, die in der Entwicklung schon weit fortgeschritten sind, möglichst breit im nationalen Impfprogrammen zu verankern. Es fehlt jedoch weitgehend an verlässlichen Daten, um den Einsatz zu rechtfertigen.
Bislang gelangten nur wenige harte Daten zur Wirksamkeit der chinesischen Impfstoffe an die Öffentlichkeit. Drei, die sich aktuell in Phase III der klinischen Erprobung befinden, beruhen auf inaktivierten Viren. Zwei davon stammen aus dem Staatsunternehmen Sinopham und einer von dem in Peking ansässigen Privatunternehmen Sinovac Biotech.
Zum Hintergrund: die „China National Pharmaceutical Group“ (Sinopharm Gruppe) verfügt über eine Untereinheit namens „China National Biotech Group“ (CNBG), die für Impfstoffe und Biowissenschaften zuständig ist. Einen der beiden Kandidaten entwickelt die CNBG zusammen mit dem „Wuhan Institute of Biological Products“ des Unternehmens („Vero cells“) und den anderen mit dem ebenfalls zur Gruppe gehörigen „Beijing Institute of Biological Products“ (BBIBP-CorV). Beide werden in Presseberichten gelegentlich verwechselt. Die einzige Adenovirus-Vakzine in Phase III stammt von CanSino Biologics (Convidicea).
| Zulassungen für COVID-19-Impfstoffe aus China (Stand 10. Februar 2021) | |||
|---|---|---|---|
| Unternehmen | Name | Zulassung in China | Weitere Zulassungen |
| Sinopharm/Wuhan Institute of Biological Products | Inactivated Novel Coronavirus Pneumonia (COVID-19) vaccine (Vero cells) Inaktiviertes Virus | Notfallzulassung | |
| Sinopharm/ Beijing Institute of Biological Products | BBIBP-CorV Inaktiviertes Virus | Notfallzulassung Bedingte Zulassung am 31. Dezember 2020 | zwölf Länder, darunter Ungarn |
Sinovac
| CoronaVac Inaktiviertes Virus | Notfallzulassung Bedingte Zulassung am 5. Februar 2021 | sechs Länder |
| CanSino Biologics/ Beijing Institute of Biotechnology, Academy of Military Medical Sciences | Convidicea (Ad5-nCoV) Vektorvakzine
| Spezielle „Militär“-Zulassung | Mexiko |
| Quelle: COVID-19 vaccine tracker, RAPS | |||
BBIBP-CorV von Sinopharm
Der Impfstoff mit Namen BBIBP-CorV hat im Dezember als erster in China eine bedingte Marktzulassung von der „National Medical Products Administration“ erhalten. Wie aus einer Unternehmensmitteilung hervorgeht, sollen über 60.000 Freiwillige mit 125 Nationalitäten an der klinischen Phase-III-Erprobung der Vakzine in Ländern außerhalb Chinas teilgenommen haben. Noch vor China hatten die Vereinigten Arabischen Emirate (VAE) und Bahrain den COVID-19-Impfstoff am 9. beziehungsweise 12. Dezember als erste Länder genehmigt. Während Sinopharm eine Wirksamkeitsrate von 79,34 Prozent angibt, kommen die VAE auf 86 Prozent.
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.